응고 - 무엇입니까, 개념, 유형, 예제, 융합
응고란 무엇인지, 어떤 종류가 있는지, 각각의 특징과 사례를 설명합니다. 또 융합이란 무엇인가.

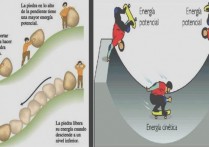
응고는 용암 냉각과 같이 온도나 압력의 변화로 인해 발생합니다.
응고란 무엇입니까?
응고란 물질이 받는 압력을 변화시켜 물질이 액체 상태 에서 고체 상태 로 변하는 물리적 변화 또는 상 변화 과정입니다 .
후자의 경우 이는 액체 물질에 대해서도 동일한 결과를 가정하지만 온도가 어는점 이하로 떨어지는 결빙과 구별됩니다 . 이 차이점은 다소 기술적이며 비학술적 또는 과학 분야에서는 두 용어가 종종 같은 의미로 사용됩니다.
응고 또는 동결은 압력 및/또는 온도의 물리적 조건 변화에 따라 고체 물질을 액체로 만드는 과정(용해 또는 용융과 반대)입니다. 이는 물질이 화학적으로 변형되지 않는다는 점에서 가역적 과정입니다 . 즉, 화학적(구성적) 변화가 발생 하지 않고 물리적(형태) 변화가 발생합니다.
문제에서 발생하는 변화에 따라 다양한 유형의 응고에 대해 이야기할 수 있습니다. 예를 들면 다음과 같습니다.
-
결정화 . 입자가 함께 모이 면서 균일한 액체 내에서 고체 구조가 형성되는 것으로 구성됩니다. 고체와 액체가 잠시 동안 공존하기 때문에 물이 얼기 시작할 때처럼 이러한 구조를 관찰하는 것이 가능합니다.
-
유리화 . 유리나 글리세롤과 같은 특정 물질은 결정화 없이 응고될 수 있으므로 한 물리적 상태와 다른 물리적 상태 사이에 갑작스러운 전이가 없고 오히려 점차적으로 탄성이 손실되어 고체 상태로 이어집니다.
-
과냉각 . 이는 액체가 응고되지 않고 상 변화 없이 어는점 이하의 온도까지 냉각되는 과정입니다. 이를 위해서는 액체가 충분히 순수해야 합니다.
참조: 물질의 상태
응고 및 융합

녹는점은 물질이 액체가 되는 온도이다.
녹는다는 것은 응고와 동결의 반대 과정입니다 . 이는 고체 물질에 에너지를 추가하여 입자 의 움직임을 증가시키고 화학 결합과 고정된 구조를 잃는 것으로 구성됩니다. 고체 상태에서 액체 상태로의 전환입니다.
각 고체 에는 상이 바뀌고 액체 상태가 되는 녹는점이 있습니다 . 이는 액체가 고체가 되는 어는점과 반대입니다. 녹는점이 높을수록 고체가 녹아 액체 또는 반액체가 되기 위해 더 많은 에너지(즉, 온도가 높아짐)가 필요합니다.
더 보기: 퓨전
응고의 예

유리는 가열되어 형태를 이루고 냉각되면 견고성을 회복합니다.
응고의 몇 가지 예는 다음과 같습니다.
-
냉장고 내부의 물이 어는 현상은 열 손실 로 인해 액체가 응고되는 전형적인 예입니다 .
-
화산 폭발 시 하층토에서 분출되는 끓는 용암은 엄청난 온도와 압력을 받는 액체 물질입니다. 표면으로 떠오르면 서서히 에너지를 잃고 결국 고체물질로 변하게 된다.
-
점토로 형상을 만들 때 우리는 점토가 젖었을 때 가단성이 있지만 건조되면 단단하고 단단하며 부서지기 쉽다는 것을 알 수 있습니다.
-
철강 산업의 금속은 거대한 용광로에서 가열되어 녹인 다음(고체 상태에서 액체 상태로 전환) 특정 모양의 주형에 부어집니다 . 거기에 담긴 액체 금속은 냉각되어 굳어지며 일단 금형에서 제거되면 원하는 모양을 갖게 됩니다.
계속하기: 역승화